Общая характеристика тяжёлых металлов. Формы нахождения тяжёлых металлов в окружающей среде
Начиная с концентрации 0,006-0,01 мг/дм3 ртуть в виде водорастворимых солей оказывает губительное влияние на рыб и другие водные организмы [20].
При отравлениях ртутью, особенно ее органическими соединениями, отчетливо выражены симптомы поражений нервной системы (парезы, параличи, нарушения зрения и слуха) [20].
Недавно было доказано, что микроорганизмы могут использовать реакции метилирования для превращения металлов в металлорганические соединения. Особое значение имеет способность некоторых микроорганизмов превращать ионы ртути в метил - и диметилртуть:
Нg2+ + донор метильной группы - > СН3 - Нg+,
СН3 - Нg+ + донор метильной группы СН3 - Нg+ - СН3.
Организмы, способные осуществлять эти реакции, в своих обычных метаболических процессах используют трансметилирование, образуя такие соединения, как метан; в этих системах могут реагировать также и металлы [20].
Метилртутные и некоторые другие ртутьорганические соединения отличаются особой токсичностью. Они растворимы в жирах, и поэтому хорошо всасываются, легко проникают через гематоэ
нцефалический барьер и приводят к нейротоксическим эффектам [1].
Соединения ртути опасны для популяций позвоночных, так как, проходя через пищевые цепи, способны повышать свою концентрацию в десятки раз (см рис.1), а вследствие длительного биологического периода полураспада медленно выводятся из организма [1].
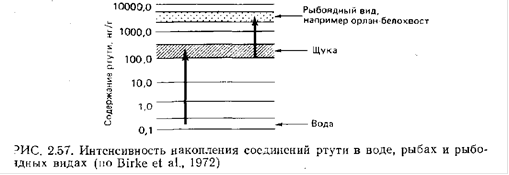
Рисунок 1. Интенсивность накопления соединений ртути в воде, рыбах и рыбоядных видах
Хром.
Ионы хрома являются непременными компонентами природных водоемов. В зависимости от условий среды (pH, окислительно-восстановительный потенциал, наличие лигандов) они существуют в разных степенях окисления и входят в состав разнообразных неорганических и металлорганических соединений, которые могут быть истинно растворенными, коллоидно-дисперсными или входить в состав минеральных и органических взвесей. Истинно растворенная формы металла, в свою очередь, весьма разнообразны, что связано с процессами гидролиза, гидролитической полимеризации (образованием полиядерных гидроксокомплексов) и комплексообразования с различными лигандами. Соответственно, как каталитические свойства металлов, так и доступность для водных микроорганизмов зависят от форм существования их в водной экосистеме.
Переход хрома в водной среде в металлокомплексную форму имеет три следствия: может происходить увеличение суммарной концентрации ионов металла за счет перехода его в раствор из донных отложений; мембранная проницаемость комплексных ионов может существенно отличаться от проницаемости гидратированных ионов; токсичность металла в результате комплексообразования может сильно измениться.
В поверхностных водах соединения хрома находятся в растворенном и взвешенном состояниях, соотношение между которыми зависит от состава вод, температуры, рН раствора. Взвешенные соединения хрома представляют собой в основном сорбированные соединения хрома. Сорбентами могут быть глины, гидроксид железа, высокодисперсный оседающий карбонат кальция, остатки растительных и животных организмов. В растворенной форме хром может находиться в виде хроматов и бихроматов. При аэробных условиях Cr (VI) переходит в Cr (III), соли которого в нейтральной и щелочной средах гидролизуются с выделением гидроксида.
В речных незагрязненных и слабозагрязненных водах содержание хрома колеблется от нескольких десятых долей микрограмма в литре до нескольких микрограммов в литре, в загрязненных водоемах оно достигает нескольких десятков и сотен микрограммов в литре [3]. Средняя концентрация в морских водах - 0.05 мкг/дм3 [12, 14, 19]. ПДК хром (III) в поверхностных водах составляет 0,005 мг/дм3, а хром (VI) - 0,001 мг/дм3 [22,23].
Цинк.
Цинк попадает в природные воды в результате протекающих в природе процессов разрушения и растворения горных пород и минералов (сфалерит, цинкит, госларит, смитсонит, каламин), а также со сточными водами рудообогатительных фабрик и гальванических цехов, производств пергаментной бумаги, минеральных красок, вискозного волокна и др. В воде цинк существует главным образом в ионной форме или в форме его минеральных и органических комплексов, иногда встречается в нерастворимых формах: в виде гидроксида, карбоната, сульфида и др.
В речных водах концентрация цинка обычно колеблется от 3 до 120 мкг/дм3, в морских - от 1,5 до 10 мкг/дм3. Содержание в рудных и особенно в шахтных водах с низкими значениями рН может быть значительным.
Цинк относится к числу активных микроэлементов, влияющих на рост и нормальное развитие организмов. В то же время многие соединения цинка токсичны, прежде всего его сульфат и хлорид [3].
ПДК цинка в поверхностных водах составляет 0,5 мг/дм3 [22,23].
Никель.
Присутствие никеля в природных водах обусловлено составом пород, через которые проходит вода: он обнаруживается в местах месторождений сульфидных медно-никелевых руд и железоникелевых руд. В воду попадает из почв и из растительных и животных организмов при их распаде. Повышенное по сравнению с другими типами водорослей содержание никеля обнаружено в сине-зеленых водорослях. Соединения никеля в водные объекты поступают также со сточными водами цехов никелирования, заводов синтетического каучука, никелевых обогатительных фабрик. Значительные выбросы никеля сопровождают сжигание ископаемого топлива.
Еще статьи
Экологическая оценка состояния окружающей природной среды под воздействием антропогенной нагрузки при строительстве и эксплуатации объекта повышенной опасности
Актуальность работы. Антропогенная деятельность
человека оценивается с помощью методов производственных процессов. Например,
строительство, землепользование, утилизация отходов являются опасными
объектами. Для их реализации необходима процедура ОВОС с последующим
прох ...